Обязательная маркировка лекарственных препаратов
Маркировка лекарств «под ключ». Организация и внедрение,
ЭДО для маркировки, выпуск ЭЦП
Тарифы
Подберите оптимальный тариф для вашего бизнеса
Усиленная квалифицированная электронная подпись
Регистрация в ЦРПТ и для работы с сервисами ЭДО
Регистрация в ЦРПТ и для работы с сервисами ЭДО
2D-сканер
Считывание кодов маркировки с товара
Считывание кодов маркировки с товара
Онлайн-кассы для работы с маркировкой
Продажа маркированных товаров и формирование актуальных чеков
Продажа маркированных товаров и формирование актуальных чеков
Услуги оператора фискальных данных
Передача информации о маркированных товарах из чека в систему «Честный ЗНАК»
Передача информации о маркированных товарах из чека в систему «Честный ЗНАК»
Электронный документооборот
Обмен УПД между контрагентами
Обмен УПД между контрагентами
Настройка рабочего места для обязательной маркировки
Работа с маркированной продукцией в соответствии с требованиями законодательства
Работа с маркированной продукцией в соответствии с требованиями законодательства
С 1 сентября 2026 года перечень медицинских изделий, подлежащих обязательной маркировке, расширяется на 14 новых категорий (Постановление Правительства РФ от 06.04.2026 № 375). Обязательная маркировка лекарственных препаратов действует с 1 июля 2020 года и к 2026 году охватывает все без исключения серийные медикаменты, поступающие в оборот на территории России. Нарушение правил грозит административными штрафами до 100 000 рублей для юридических лиц по ст. 6.34 КоАП РФ (нарушение порядка маркировки лекарств) и до 300 000 рублей по ч. 2 ст. 15.12 КоАП РФ (продажа, хранение, перевозка немаркированной продукции), а при крупном обороте — уголовной ответственностью по ст. 171.1 УК РФ.
Ниже разобраны ключевые требования к участникам оборота, алгоритм подключения к системе мониторинга, порядок работы с остатками и поврежденными кодами, а также практические ситуации, которые чаще всего вызывают вопросы у аптек, клиник и дистрибьюторов.
Что такое маркировка лекарств и зачем она нужна
Каждая вторичная (потребительская) упаковка лекарственного препарата должна содержать уникальный двумерный штрихкод формата Data Matrix. Система маркировки лекарственных препаратов устроена так: код генерирует оператор «Честный знак» (ЦРПТ), а наносит его производитель или импортер до ввода товара в оборот.
Код связывает физическую упаковку с записью в информационной системе мониторинга движения лекарственных препаратов (ИС МДЛП). Каждая операция с упаковкой (отгрузка, приемка, продажа, списание) фиксируется в системе. Результат: государство, участники рынка и конечный потребитель через мобильное приложение могут проверить происхождение, маршрут и подлинность конкретной единицы товара.
Структура кода маркировки
Код маркировки лекарственного препарата состоит из двух частей:
- Код идентификации: международный код товара GTIN (14 символов) + индивидуальный серийный номер (13 символов). GTIN и серийный номер дублируются в виде читаемого текста на упаковке.
- Код проверки (криптохвост): ключ (4 символа) + значение кода (44 символа). Позволяет проверить легальность оборота препарата.
Data Matrix наносится на вторичную (потребительскую) упаковку. При отсутствии вторичной упаковки — на первичную (блистер, ампулу) или на неотделяемую этикетку. На транспортную (третичную) тару наносится групповой штрихкод.
Цели системы
Федеральный закон от 28.12.2017 № 425-ФЗ закрепил три основные задачи:
- Противодействие обороту контрафактных и фальсифицированных лекарств.
- Контроль ценообразования на препараты из перечня ЖНВЛП.
- Обеспечение прослеживаемости от производителя до пациента, включая адресное распределение льготных медикаментов.
Когда и зачем ввели маркировку лекарственных препаратов
| Дата | Событие | Основание |
| Февраль 2017 | Старт эксперимента по маркировке лекарств | Постановление Правительства РФ от 24.01.2017 № 62 |
| 1 октября 2019 | Обязательная маркировка препаратов из перечня ВЗН (7 высокозатратных нозологий) | Постановление Правительства РФ от 14.12.2018 № 1556 |
| 1 июля 2020 | Обязательная маркировка всех лекарственных препаратов | Постановление Правительства РФ от 14.12.2018 № 1556 (во исполнение Федерального закона от 28.12.2017 № 425-ФЗ) |
| 1 сентября 2026 | Расширение маркировки на медицинские изделия (перчатки, шприцы, маски, томографы и др.) | Постановление Правительства РФ от 06.04.2026 № 375 |
Важно! Постановление № 375 касается именно медицинских изделий, а не лекарственных препаратов. Для лекарств правила маркировки лекарственных препаратов действуют с 2020 года. Однако для работы с медизделиями потребуется подключить новую товарную группу в личном кабинете «Честного знака» и обновить товароучетные системы.
Перечень лекарственных препаратов, подлежащих маркировке
Общее правило
Маркировке подлежат все лекарственные препараты, зарегистрированные в Государственном реестре лекарственных средств и произведенные (ввезенные) после 1 июля 2020 года. Форма выпуска, рецептурный статус и ценовая категория значения не имеют.
Исключения
Закон и подзаконные акты выводят из-под маркировки узкий перечень случаев:
- Лекарства, произведенные до 1 июля 2020 года, если срок годности еще не истек (реализация без маркировки допускается до окончания срока годности).
- Препараты, предназначенные для экспорта (вывозимые за пределы ЕАЭС).
- Фармацевтические субстанции (не являются готовыми лекарственными формами).
- Экстемпоральные (внутриаптечные) препараты, изготовленные по рецепту врача в аптеке (не серийное производство).
- Радиофармацевтические лекарственные препараты с коротким периодом полураспада, для которых нанесение кода технически невозможно.
- Лекарственные препараты, предназначенные для проведения клинических исследований.
Гомеопатические препараты
Если гомеопатический препарат зарегистрирован в ГРЛС и выпускается серийно, он подлежит маркировке на общих основаниях. Исключений для гомеопатии закон не предусматривает.
Рекламные образцы
Образцы лекарственных препаратов, распространяемые бесплатно для рекламных целей, формально вводятся в оборот. Если они имеют регистрационное удостоверение и серийную упаковку, маркировка обязательна. Вывод из оборота фиксируется как «безвозмездная передача» или «использование для собственных нужд».
Кто участвует в маркировке лекарств
Кто участвует в маркировке лекарств
Производители и импортеры
Наносят код Data Matrix на упаковку, передают сведения о вводе в оборот через регистратор эмиссии, формируют электронные документы для дистрибьюторов через систему ЭДО.

Дистрибьюторы и оптовые поставщики
Подтверждают приемку партий через ЭДО (сверка кодов с электронной накладной), передают сведения об отгрузке следующему звену цепочки.
Аптечные организации
Аптека подтверждает приемку, при розничной продаже сканирует код на кассе. Через оператора фискальных данных (ОФД) информация о выбытии поступает одновременно в ФНС и ИС МДЛП.
Медицинские учреждения
Подтверждают приемку. Вывод из оборота (использование при оказании медпомощи, льготный отпуск) фиксируется через регистратор выбытия, который ЦРПТ предоставляет бесплатно.
Исключения: Регистратором выбытия не оснащаются медицинские организации, подведомственные Минобороны России; кабинеты врачебной помощи в образовательных учреждениях, являющиеся структурными подразделениями медорганизации; обособленные подразделения, получающие лекарства из головной медорганизации; аптечные организации, не отпускающие продукцию бесплатно по рецепту.
Как начать работу с маркировкой лекарственных препаратов: инструкция
Алгоритм для организации, которая еще не зарегистрирована в системе:
1
2
3
4
5
Что нужно аптеке
| Элемент | Назначение |
| УКЭП | Подписание электронных документов, вход в ЛК |
| 2D-сканер | Считывание Data Matrix при приемке и продаже |
| Онлайн-касса | Передача данных о розничной продаже в ОФД и МДЛП |
| ОФД (оператор фискальных данных) | Передача фискальных данных и сведений о выбытии в ФНС и ИС МДЛП |
| ЭДО | Обмен УПД с поставщиками |
| Товароучетная система | Сверка кодов, инвентаризация |
Обратите внимание: с 1 июня 2025 года розничные продавцы лекарственных препаратов обязаны применять разрешительный режим на кассах. Без этого работа с маркированными лекарствами может привести к нарушениям действующего законодательства.
Перечень препаратов, на которые режим не распространяется, закреплен в части 7.1 статьи 67 Федерального закона «Об обращении лекарственных средств».
Что нужно медучреждению
| Элемент | Назначение |
| УКЭП | Регистрация и подписание |
| 2D-сканер | Приемка товара |
| Регистратор выбытия | Фиксация использования препарата (предоставляется бесплатно ЦРПТ) |
| ЭДО | Подтверждение поставок |
Алгоритм работы с маркированными лекарственными препаратами
Немаркированные остатки
Лекарства, произведенные до 1 июля 2020 года, допускается реализовывать без маркировки до истечения срока годности. Никаких дополнительных действий с ними предпринимать не требуется. Если срок годности истек, препарат подлежит утилизации по общим правилам.
Поврежденный код маркировки
Если код на упаковке не считывается (стерт, поврежден, залит), участник оборота не вправе продавать или передавать такой товар дальше по цепочке. Порядок действий:
- Связаться с поставщиком и оформить возврат с указанием причины «повреждение средства идентификации».
- Поставщик (или производитель) перемаркирует товар: заказывает новый код в системе, наносит его на упаковку, регистрирует повторный ввод в оборот.
- Если возврат поставщику невозможен, аптека может самостоятельно инициировать перемаркировку, заказав новые коды через личный кабинет в ИС МДЛП. Для этого нужно указать GTIN и серийный номер поврежденной упаковки.
Важно! Продажа лекарства с нечитаемым кодом через кассу технически невозможна: онлайн-касса не пропустит товар без валидного кода маркировки.
Возвратный товар без этикетки
При возврате от покупателя аптека обязана повторно ввести препарат в оборот. Если физический код утрачен, необходимо запросить новый код в ИС МДЛП, распечатать и нанести на упаковку. Без этой процедуры повторная реализация незаконна.
Интернет-аптеки и безналичный расчет
Аптеки, работающие дистанционно (интернет-аптеки с доставкой), подчиняются тем же правилам маркировки препаратов. При отпуске товара курьеру или при вручении покупателю код сканируется на кассе, данные уходят в ОФД и МДЛП. Форма расчета (наличный, безналичный, онлайн-оплата) на обязанность маркировки не влияет.
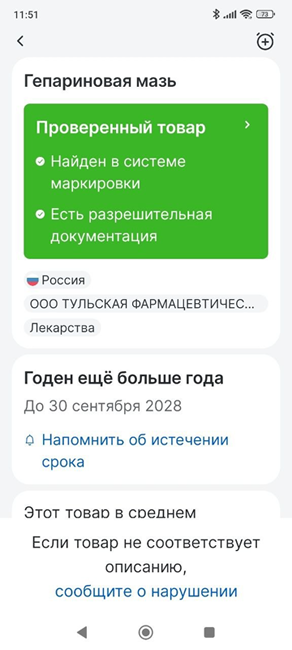
Проверка подлинности лекарства через приложение Честный знак по коду Data Matrix
Что нужно для обязательной маркировки лекарств
Правила маркировки лекарственных препаратов предусматривают онлайн-проверку подлинности через мобильное приложение «Честный знак» (доступно для iOS и Android): достаточно навести камеру на код Data Matrix, чтобы получить наименование препарата, производителя, серию, срок годности и текущий статус (в обороте или выведен). Если код не найден в системе или уже выведен из оборота, это сигнал о возможном контрафакте. В таком случае приложение предлагает подать жалобу в Росздравнадзор.
Офлайн-проверка возможна через торговое оборудование участников оборота: при сканировании кода на кассе или терминале приемки система сверяет данные с ИС МДЛП и подтверждает или блокирует операцию.
Особенности маркировки лекарств
Расширение на медицинские изделия
Постановление Правительства РФ от 06.04.2026 № 375 добавило в перечень обязательной маркировки медицинские изделия: перчатки, шприцы, маски, пробирки, салфетки, слуховые аппараты, компьютерные томографы, коронарные стенты, аппараты ИВЛ, инкубаторы для новорожденных, импланты (филлеры, косметологические нити) и другие позиции.
Сроки поэтапного внедрения для медизделий (требуют верификации по тексту постановления на publication.pravo.gov.ru):
- С 1 сентября 2026 года: производители и импортеры передают сведения о вводе в оборот.
- С 1 марта 2027 года: передача сведений о выводе из оборота (включая розничную продажу через ККТ).
- С 1 сентября 2027 года: передача сведений об обороте, включая оптовые операции.
Нереализованные остатки медизделий, имеющиеся на складах на 1 сентября 2026 года, можно продавать без маркировки до окончания срока годности либо промаркировать и внести в систему до 31 мая 2027 года.
Что это значит для аптек и клиник
Организации, уже зарегистрированные в системе «Честный знак» для работы с лекарственными препаратами, не должны создавать новую учетную запись. Однако для работы с медицинскими изделиями необходимо подключить соответствующую товарную группу в личном кабинете, настроить товароучетные системы для корректной работы с новыми атрибутами (для масок, например, нужно указывать одноразовость, размер и основной материал) и обновить ЭДО-интеграции.
Честный знак маркировка лекарств и медизделий ведется в единой инфраструктуре: участникам рынка, уже подключенным к системе, потребуется лишь расширить перечень товарных групп, а не выстраивать процессы заново.
Код Data Matrix на упаковке лекарства с расшифровкой полей:
Штрафы за отсутствие маркировки
Ответственность за нарушения в сфере маркировки лекарственных препаратов установлена ст. 6.34 КоАП РФ (нарушение порядка маркировки и передачи данных в систему мониторинга; введена Федеральным законом от 15.04.2019 № 58-ФЗ), ч. 2 ст. 15.12 КоАП РФ (оборот немаркированной продукции) и ст. 171.1 УК РФ (при крупном и особо крупном размере).
| Нарушение | Штраф для должностных лиц | Штраф для юридических лиц | Основание |
| Несвоевременное нанесение маркировки или нарушение порядка нанесения средств идентификации на лекарства | от 5 000 до 10 000 руб. | от 50 000 до 100 000 руб. | ч. 1 ст. 6.34 КоАП РФ |
| Непредоставление или несвоевременное предоставление сведений в систему мониторинга | от 5 000 до 10 000 руб. | от 50 000 до 100 000 руб. | ч. 2 ст. 6.34 КоАП РФ |
| Продажа, хранение, перевозка лекарств без маркировки | от 5 000 до 10 000 руб. | от 50 000 до 300 000 руб. с конфискацией | ч. 2 ст. 15.12 КоАП РФ |
| Ввод в оборот без маркировки в крупном размере | до 300 000 руб. или лишение свободы до 3 лет | — | ч. 1 ст. 171.1 УК РФ |
| То же в особо крупном размере | до 500 000 руб. или лишение свободы до 5 лет | — | ч. 2 ст. 171.1 УК РФ |
Помимо штрафов, немаркированная продукция подлежит конфискации.
Важно! Росздравнадзор проводит контрольные закупки и мониторинг ИС МДЛП. Несвоевременная передача данных (например, неподтверждение приемки в течение нескольких дней) пока не влечет автоматического штрафа, но создает расхождения в системе, которые привлекают внимание при плановых проверках.
Частые вопросы о маркировке лекарств
Ответственность лежит на производителе (для отечественных лекарств) или на организации, осуществляющей ввоз (для импортных). Дистрибьюторы и аптеки код не наносят, но обязаны контролировать его наличие и читаемость при приемке.
Наносить маркировку медучреждение не должно: это обязанность производителя. Но фиксировать выбытие из оборота при использовании препарата для лечения пациента обязательно. Для этого применяется регистратор выбытия, предоставляемый ЦРПТ бесплатно.
Да. Аптеки, работающие дистанционно, подчиняются тем же правилам. Форма расчета на обязанность маркировки не влияет.
Реализовывать до окончания срока годности без ограничений. Дополнительной маркировки таких остатков закон не требует. Это правило действует для лекарств, произведенных до 1 июля 2020 года.
При возврате от покупателя аптека обязана повторно ввести препарат в оборот. Если физический код утрачен, необходимо запросить новый код в ИС МДЛП, распечатать и нанести на упаковку. Без этой процедуры повторная реализация незаконна.
Любой покупатель может скачать бесплатное приложение «Честный знак» (доступно для iOS и Android), навести камеру на код Data Matrix и получить информацию: наименование препарата, производитель, серия, срок годности, текущий статус (в обороте или выведен). Если код не найден в системе или уже выведен из оборота, это сигнал о возможном контрафакте.
Нет. Экстемпоральные (внутриаптечные) лекарственные формы не являются серийно произведенными препаратами и не подлежат маркировке в ИС МДЛП. Однако ингредиенты (фармацевтические субстанции и готовые препараты), использованные при изготовлении, должны быть корректно выведены из оборота.
Образцы лекарственных препаратов, распространяемые бесплатно для рекламных целей, формально вводятся в оборот. Если они имеют регистрационное удостоверение и серийную упаковку, маркировка обязательна. Вывод из оборота фиксируется как «безвозмездная передача» или «использование для собственных нужд».
Аптека вправе отказать в приемке и вернуть товар поставщику для перемаркировки. Если возврат невозможен, аптека самостоятельно запрашивает новый код через личный кабинет ИС МДЛП, распечатывает его и наклеивает на упаковку. Реализация товара с нечитаемым кодом запрещена.
Подключитесь к системе маркировки самостоятельно
1
Оставьте заявку
Специалист проконсультирует и подберет под вашу специфику необходимое ПО и оборудование
2
Оплатите счет
После оплаты специалисты подготовят вашу компанию для работы с системой маркировки
3
Работайте с удовольствием
Принимайте и реализуйте маркированные товары
1
Оставьте заявку
2
Оплатите счет
3
Работайте с удовольствием
Специалист проконсультирует и подберет под вашу специфику необходимое ПО и оборудование
После оплаты специалисты подготовят вашу компанию для работы с системой маркировки
Принимайте и реализуйте маркированные товары
Видео
Сравнение 2D сканеров для маркировки товаров 2020г. АТОЛ, Honeywell, Mercury. Прошивка сканера АТОЛ.
Эвотор Маркировка пошаговая инструкция. Настройка, регистрация, продаем маркированную обувь.
Маркировка АТОЛ 91Ф пошаговая инструкция. Настройка, прошивка, продаем маркированную обувь.
Узнайте ответы на интересующие вас вопросы
Оставить заявку
Оставьте контактные данные, и мы вам перезвоним.